Logam mempunyai sifat dapat menghantarkan panas dan listrik, dapat ditempa, warnanya mengkilap, mempunyai titik leleh dan titik didih tinggi dan dapat membentuk aliansi dengan logam lain serta tersusun dalam kristal logam.Yang menjadi pertanyaan adalah ikatan apakah yang terdapat di antara atom-atom logam dalam kisi kristalnya?
Ikatan ionis tidak mungkin terdapat di antara atom-atom logam, karena tidak mungkin pula terjadi perpindahan elektron dari satu atom logam ke atom yang sejenis. Ikatan kovalen juga tidak mungkin berbentuk, karena dalam kristal logam, ternyata sebuah atom dikelilingi oleh 8 atau 12 atom yang lain, sedangkan valensi elektron dari logam-logam adalah 1, 2, 3 atau 4.
Untuk menjelaskan berbagai sifat logam, dikemukakan salah satu teori mengenai ikatan yang terdapat di anatara atom-atom logam yaitu teori awan elektron. Teori awan elektron atau elektron bebas ini dikemukakan oleh Drude dan Lorentz pada awal abad ke-20. Menurut teori ini di dalam kristal logam, setiap atom melepaskan elektron valensinya sehingga membentuk awan elektron dan kation yang bermuatan positif dan tersusun rapat dalam awan elektron tersebut. Ion logam yang bermuatan positif tersebut terdapat pada jarak terttentu satu sama lain dalam kristalnya. Karena elektron valensi tidak terikat pada salah satu ion logam atau pasangan ion logam, tapi terdelokalisasi terhadap semua ion logam, maka elektron valensi tersebut bebas bergerak ke seluruh bagian dari kristal logam, sama halnya dengan molekul-molekul gas yang dapat bergerak dengan bebas dalam ruangan tertentu.
Ikatan ionis tidak mungkin terdapat di antara atom-atom logam, karena tidak mungkin pula terjadi perpindahan elektron dari satu atom logam ke atom yang sejenis. Ikatan kovalen juga tidak mungkin berbentuk, karena dalam kristal logam, ternyata sebuah atom dikelilingi oleh 8 atau 12 atom yang lain, sedangkan valensi elektron dari logam-logam adalah 1, 2, 3 atau 4.
Untuk menjelaskan berbagai sifat logam, dikemukakan salah satu teori mengenai ikatan yang terdapat di anatara atom-atom logam yaitu teori awan elektron. Teori awan elektron atau elektron bebas ini dikemukakan oleh Drude dan Lorentz pada awal abad ke-20. Menurut teori ini di dalam kristal logam, setiap atom melepaskan elektron valensinya sehingga membentuk awan elektron dan kation yang bermuatan positif dan tersusun rapat dalam awan elektron tersebut. Ion logam yang bermuatan positif tersebut terdapat pada jarak terttentu satu sama lain dalam kristalnya. Karena elektron valensi tidak terikat pada salah satu ion logam atau pasangan ion logam, tapi terdelokalisasi terhadap semua ion logam, maka elektron valensi tersebut bebas bergerak ke seluruh bagian dari kristal logam, sama halnya dengan molekul-molekul gas yang dapat bergerak dengan bebas dalam ruangan tertentu.

Jadi menurut teori ini, kristal logam terdiri dari kumpulan ion logam bermuatan positif di dalam larutan elektron yang mudah bergerak. Ikatan logam terdapat antara ion logam positif dan elektron yang mudah bergerak tersebut. Teori awan elektron ini dapat menjelaskan berbagai sifat fisika logam yaitu :
1. Sifat mengkilap
Bila cahaya tampak jatuh pada permukaan logam, sebagian elektron valensi yang mudah bergerak tersebut akan tereksitasi. Ketika elektron yang tereksitasi tersebut kembali kepada keadaan dasarnya, maka energi cahaya dengan panjang gelombang tertentu (di daerah cahaya tampak) akan dipancarkan kembali. Peristiwa ini dapat menimbulkan sifat kilap yang khas untuk logam.
2. Daya hantar listrik Daya hantar listrik pada logam, disebabkan karena adanya elektron valensi yang mudah bergerak. elektron-elektron valensi tersebut bebas bergerak dalam medan listrik yang ditimbulakan sumber arus sehingga listrik dapat mengalir melalui logam.
3. Daya hantar panas
Sama halnya dengan daya hantar listrik, daya hantar panas juga disebabkan adanya elektron yang dapat bergerakn dengan bebas. bila bagian tertentu dipanaskan, maka elektron-elektron pada begian logam tersebut akan menerima sejumlah energi sehingga energi kinetisnya bertambah dan gerakannya makin cepat. Elektron-elektron yang bergerak dengan cepat tersebut menyerahkan sebagian energi kinetisya kepada elektron lain sehingga seluruh bagian logam menjadi panas dan naik suhunya.
4. Dapat ditempa, dibengkokkan dan ditarik
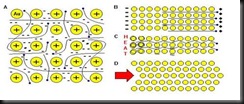
Karena elektron valensi mudah bergerak dalam kristal logam, maka elektron-elektron tersebut mengelilingi ion logam yang bermuatan positif secara simetri, karena gaya tarik antara ion logam dan elektron valensi sama kesegala arah. Ikatan dalam kisi kristal logam tidak kau seperti pada ikatan dalam senyawa kovalen, sebab dalam kisi kristal logam tidak terdapat ikatan yang terlokalisasi.
Karena gaya tarik setiap ion logam yang bermuatan positif terhadap elektron valensi sama besarnya, maka suatu lapisan ion logam yang bermuatan positif dalam kisi kristal mudah bergeser.
Bila sebuah ikatan logam putus, maka segera terbentuk ikatan logam baru. karena itu logam dapat ditempa menjadi sebuah lempeng yang sangat tipis dan ditarik menjadi kawat yang halus dan dibengkokkan.
referensi:
Syarifudin, Nuraini. 1994. IKATAN KIMIA. Yogyakarta: Gadjah mada University Press
http://permani-try.blogspot.com
No comments:
Post a Comment